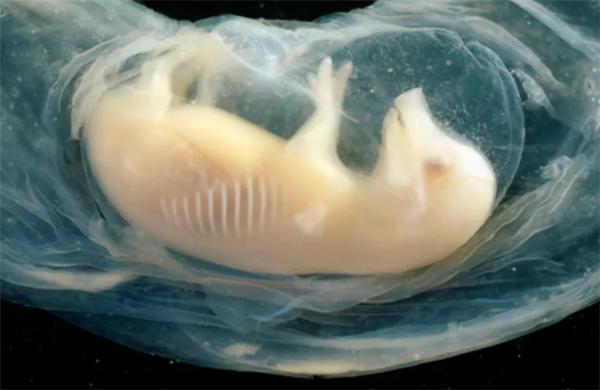
中国科学家在猪胚胎中成功培育出含人类细胞的心脏
中国科学家在猪胚胎中成功培育出含人类细胞的心脏,这一突破性进展为全球器官短缺问题提供了新的解决思路。
1. 研究核心成果
- 技术突破:中国科学院广州生物医药与健康研究院赖良学团队利用人-动物嵌合体技术,通过基因编辑敲除猪胚胎中两个心脏发育关键基因,并在桑椹胚阶段注入经过基因增强的人类干细胞,最终培育出含人类细胞的心脏组织。嵌合胚胎在代孕母猪体内最长存活21天,发育出的心脏约指尖大小,并开始自主跳动。
- 细胞整合:荧光标记显示人类细胞存在于心脏组织中,但具体比例未公布。此前该团队在猪肾脏实验中人类细胞占比达40%-60%。
2. 科学意义与潜在应用
- 解决器官短缺:全球器官移植供需严重失衡(如中国移植率仅5.6例/百万人),猪因器官大小生理结构与人类相似,被视为理想供体来源。此项技术若成熟,可规模化培育人类兼容器官。
- 技术路径优化:研究通过基因重编程增强人类干细胞在猪体内的存活能力,并利用胚胎互补原理创造“空位”促进人类细胞整合,为再生医学开辟新途径。
3. 挑战与争议
- 技术瓶颈:人类细胞仅局部分布于心脏,与猪细胞的整合程度不明确;需确保器官完全由人类细胞构成以避免免疫排斥。此外,胚胎存活时间有限(21天),人类细胞可能干扰猪心脏功能。
- 伦理与安全:跨物种嵌合体可能引发伦理争议,如人类细胞是否影响猪的神经或生殖系统。目前研究未发现人类细胞扩散至胚胎其他关键组织。
4. 国际研究背景
- 异种移植进展:此前美国已开展基因编辑猪心脏移植人体手术(患者存活2个月),中国团队亦完成猪肝脏移植脑死亡受体实验。此次嵌合心脏研究为器官培育而非直接移植,属于不同技术路线。
- 未来方向:需延长器官发育时间提高人类细胞占比,并验证功能完整性。团队计划拓展至胰腺等其他器官研究。
5. 社会影响与展望
- 临床前景:专家预测异种移植或在2025年进入临床试验阶段,但嵌合体技术仍需多年优化才能应用于临床。
- 科研生态:该研究尚未经同行评议,但已引发国际关注,被视为异种移植领域的里程碑。
这一成果标志着中国在异种器官研究领域的领先地位,尽管前路挑战重重,其潜在价值已为医学界带来曙光。