研究人员揭示胞外囊泡在肝癌转移中的新作用为肝癌早期诊断和治疗提供新靶点
研究背景
肝癌是全球最常见的恶性肿瘤之一,每年有超过84万个新症,在中国大陆和香港尤其普遍。每年香港新增约1,800肝癌病例,而每年因肝癌死亡的数目更高达1,500人。全港约8%人口是乙肝病毒(HBV)携带者,而80%肝癌病人都与HBV感染有关。肝癌的高死亡率基于缺乏早期诊断手段,以及癌细胞极易转移和复发。多数晚期确诊者已经错失手术治疗的黄金机会,余下治疗方法也十分有限。由此可见,研究重点应着重于寻找早期诊断的生物指标以及探索新的治疗方法。
研究发现
研究团队通过小鼠模型,发现肝癌细胞来源的胞外囊泡(EVs)加促了肿瘤的生长和向肺部转移。研究团队进一步发现EVs中的nidogen 1(NID1)对于EVs加促肿瘤生长及转移的作用至关重要。从功能上来说,EV-NID1能增生血管,并激活成纤维细胞,分泌出肿瘤坏死因子受体1(TNFR1),令肿瘤细胞在肺部定植。此外,EV-NID1还会加剧肿瘤细胞的增殖、转移和侵袭性。抑制EV-NID1的表达可大幅度降低EVs促进肿瘤生长及转移的作用。在小鼠实验中,利用抗TNFR1抗体可以有效地减轻肝癌EVs诱导的肿瘤肺部转移。而在临床观察中,肝癌病人血清EV-NID1和TNFR1的含量都较正常对照组为高。
领导这项研究的病理学系副教授任蕙苹博士表示:「这次研究结果首度在肝癌病人的胞外囊泡中找到了NID1,并证实EV-NID1在促进肝癌发展和转移至肺部的一个未知功能。我们希望靠堵截肿瘤细胞来源胞外囊泡的传送及其信号通道,为未来肝癌治疗提供一种新选择和方法。」
研究意义
该研究发现对于肝癌的临床治疗具重要意义。首先,团队鉴定了肝癌的始动分子,为设计新疗法立下根基。其次,在肝癌病人的样本中,发现其血清EV-NID1和TNFR1的表达水平与其肿瘤分期正向相关,说明了这两个分子有望作为肝癌早期诊断的非侵入型生物指标。最后,该研究提供了治疗肝癌的新方向,通过标靶肿瘤性的EVs及其介导的通路,为肝癌病人提供新的治疗选择。
关于研究团队
这项研究由港大医学院病理学系副教授任蕙苹博士领导。港大医学院病理学系博士后研究员毛晓雯博士和郑思强博士为论文的共同第一作者,并由研究助理杨乐心小姐和邝文诺先生协助。其他参与研究的包括香港大学化学系质谱设备经理冯依文博士;港大医学院病理学系和生物医学学院助理教授钟亦琛博士;港大医学院内科学系助理教授王嘉豪博士、临床助理教授麦龙儿医生、临床副教授何重文医生,以及肠胃及肝脏科讲座教授、李树芬医学基金会基金教授(内科)、副系主任袁孟峰教授;港大医学院公共卫生学院前副教授彭希文博士,以及港大医学院病理学系首席临床讲师王碧医生。合作机构包括香港理工大学、伊利沙伯医院和广州南方医科大学。
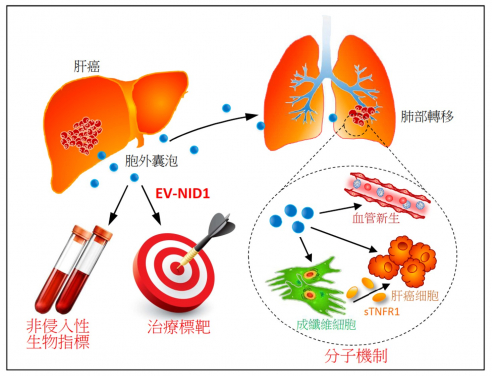
香港大学李嘉诚医学院(港大医学院)研究团队发现,肿瘤来源的胞外囊泡加速肝癌转移。这项崭新发现为肝癌治疗提供了新的生物指标及治疗方向。相关研究成果已于国际权威跨领域科学期刊《尖端科学》发表。


