开辟新冠mRNA疫苗开发的全新领域:发现mRNA诱导小鼠体内产生新冠病毒样颗粒强烈激活免疫系统
目前针对新冠病毒的疫苗研发工作正在全球多国开展。由于新冠病毒本身的特殊性,用mRNA表达抗原,既能够快速有效激活免疫系统,又不会引发非特异性的不良免疫反应,但仍需要深入系统的研究。
近日,复旦大学生命科学学院教授林金钟团队联合上海交通大学、上海蓝鹊生物医药有限公司(蓝鹊生物)以及厦门大学等团队合作,在《细胞研究》(Cell Research)杂志上在线发表了题为《一种编码SARS-CoV-2病毒样颗粒的COVID-19 mRNA疫苗在小鼠中诱导强烈的抗病毒样免疫反应》(“A COVID-19mRNA vaccine encoding SARS-CoV-2 virus-like particles induces a strong antiviral-like immune response in mice”)的研究成果。林金钟团队利用蓝鹊生物高通量mRNA合成筛选平台,设计了多种针对新冠的mRNA疫苗方案,研究发现用mRNA表达的新冠病毒样颗粒可以在小鼠体内诱导产生更强的特异专一免疫反应。这是全世界首个使用mRNA技术进行体内表达新冠病毒样颗粒并完成概念疫苗验证的研究,将开辟新冠mRNA疫苗开发的全新领域。
继2月底在国际上首次报道利用mRNA技术体外得到病毒样颗粒的结果后,林金钟团队系统研究了mRNA序列和修饰优化对新冠蛋白表达的重要作用,利用蓝鹊生物独有的mRNA VLP技术平台,设计了三种mRNA疫苗方案,即用mRNA表达了新冠病毒S蛋白的RBD片段、S蛋白全长以及同时表达三种蛋白S、M、E,并最终由这三种蛋白在体内自组装成新冠病毒样颗粒。病毒样颗粒(Virus Like Particles,简称VLP)就是外表类似病毒的颗粒,具有完整的病毒衣壳和新冠特有的棘突,但不包含病毒的任何遗传信息,不能进行复制,本身完全无毒。
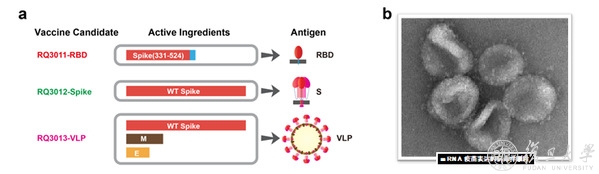
图1.a.三种mRNA疫苗设计方案;b.用mRNA疫苗表达的病毒样颗粒(VLP,电镜照片),与天然病毒极为相似。
研究团队通过比较mRNA序列和修饰方式对蛋白翻译的影响,对三种mRNA疫苗分别做了系统性的优化和筛选,从上百种候选方案中,选取了表达量最高、注射剂量相对较低的mRNA疫苗进行动物免疫,并比较了这3种mRNA疫苗在小鼠中诱导中和抗体的情况。
实验结果显示,产生病毒样颗粒的疫苗RQ3013-VLP在小鼠体内诱导出的中和抗体,首次注射4周后,已达到疫苗RQ3012-Spike(疫苗只编码S蛋白)诱导的中和抗体的2.5倍,并具有显著差异。更为重要的是,疫苗RQ3013-VLP产生的中和抗体在注射8周后,仍在持续上升,显示了这种疫苗可能会提供长效保护机制。这是因为病毒样颗粒与病毒形态最接近,在体内稳定性优于单独的S蛋白,病毒样颗粒如同用mRNA方法给新冠病毒精准画像,从而保证了免疫系统能够正确识别真正的病毒。同时,病毒样颗粒的组成成分可通过mRNA编码和比例进行调控,在应对病毒突变方面更具有优势。研究验证了mRNA诱导产生病毒样颗粒作为疫苗的优势,为后续临床实验打下了坚实基础,同时也为打造安全高效、可应对多种变化的新型疫苗提供了新方向。
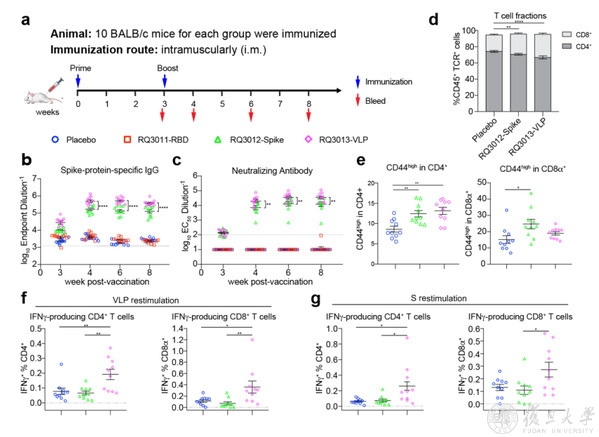
图2. a.小鼠免疫示意图; b-c.三种疫苗诱导的结合抗体和中和抗体的差别;d-g.疫苗RQ3012-Spike和疫苗RQ3013-VLP激活的T细胞免疫比较。
复旦大学生命科学学院教授院林金钟团队一直致力于蛋白翻译调控研究。本项目得到复旦大学新冠肺炎应急基金、上海市市级科技重大专项、上海交大新冠肺炎专项基金和国家自然科学基金的支持。


