科研人员首次在全CNS尺度上实现异源性小胶质细胞替换/移植
小胶质细胞是中枢神经系统(CNS)内重要的免疫细胞,携带有基因突变的小胶质细胞参与了多种神经退行性病变的发生和发展。常规的基因治疗思路无法用于小胶质细胞,主要原因是由于常用的非整合类病毒载体(如AAV)无法感染小胶质细胞,以及少数的整合类病毒载体(如lentivirus)虽然能够感染小胶质细胞,但只能影响注射位点附近的局部范围,无法在全脑尺度上对小胶质细胞进行操控。因此,如何在全脑范围内进行操控成为限制小胶质细胞基因治疗的瓶颈。研究人员提出了可以通过细胞移植将外源性细胞替换原生小胶质细胞的设想,然而其替换效率极低或宿主必须为特定的转基因动物(且必须在发育早期完成替换),因此无法真正运用于医疗实践。
2018年2月,脑科学转化研究院研究员彭勃课题组在Nature Neuroscience和Cell Discovery发表两篇通讯作者论文,阐明了中枢神经系统内小胶质细胞再殖(microglia repopulation)的起源,并发现小胶质细胞具有惊人的自我更新潜能。近日,课题组进一步以再殖现象为基础,开发了三种用外源性细胞替换原生小胶质细胞的移植方案,并在全CNS范围内实现了高效地细胞替换。8月11日,研究成果以“Efficient strategies for microglia replacement in the central nervous system”为题在线发表于Cell Reports。
小胶质细胞替换:领域内的难题
彭勃课题组发现,通过传统骨髓移植(traditional bone marrow transplantation, tBMT)方法,外源性骨髓细胞可以进入中枢神经系统并分化成小胶质细胞样细胞(microglia-like cell)。然而,其细胞替换的效率很低,仅有约2%的小胶质细胞被外源性细胞替换,无法达到满足细胞治疗的目的。此外,通过颅内注射的方式向脑内移植小胶质细胞(traditional microglia transplantation, tMT),仅有极少数的小胶质细胞能够整合入脑内,约占脑内细胞总数的0.03%。
近年来,国际上有多个课题组通过相似的思路实现小胶质细胞移植:在发育早期(P0~P1)将外源性小胶质细胞移植入免疫缺陷的小鼠。但是,该类方法依赖于免疫缺陷型的移植受体小鼠,且移植必须在发育早期完成(小胶质细胞未在脑内完成定殖时),无法用于疾病治疗。因此,如何能在成年小鼠脑内高效地替换小胶质细胞成为领域内关注的重点问题。
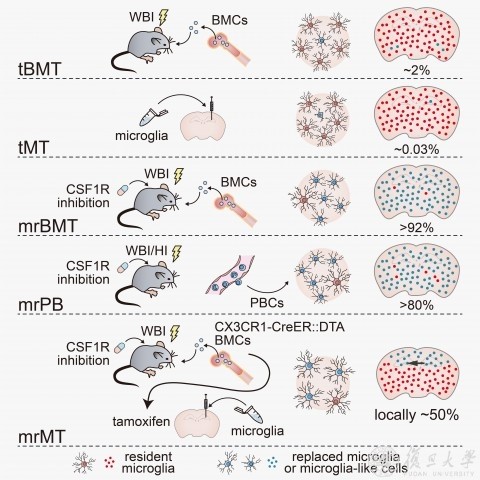
三种全新的小胶质细胞高效替换方案
彭勃课题组开发了三种不同的小胶质细胞替换方案。课题组利用药物特异性抑制集落刺激因子1受体(CSF1R),高效清除CNS内的小胶质细胞,同时不引起副作用。随后,再进行骨髓移植。外源性的骨髓细胞可进入脑内并分化成小胶质细胞样细胞,替换效率超92%。同样,几乎所有的视网膜和脊髓的小胶质细胞被外源性细胞所替换。该方案命名为mrBMT(microglia replacement by bone marrow transplantation)。
虽然mrBMT可以以极高的效率在全CNS范围内替换小胶质细胞,但使用的供体细胞为骨髓细胞,捐献来源较为有限,将影响其在未来疾病治疗上的普及。因此,课题组进一步开发了新的小胶质细胞替换方案,能将血液细胞诱导分化为小胶质细胞样细胞,并高效替换CNS的原生小胶质细胞(替换效率>80%)。该方案命名为mrPB(microglia replacement by peripheral blood)。
然而,mrBMT和mrPB细胞更多地保留有外周巨噬细胞的特征,与CNS的小胶质细胞存在一定差异。此外,在某些特定的情况下,需要替换特定脑区的小胶质细胞,而不影响其他脑区。于是,课题组进一步开发了第三种方案mrMT(microglia replacement by microglia transplantation)。该方案可将外源小胶质细胞高效替换特定局部脑区的原生小胶质细胞,同时移植的细胞保留CNS小胶质细胞的特征。
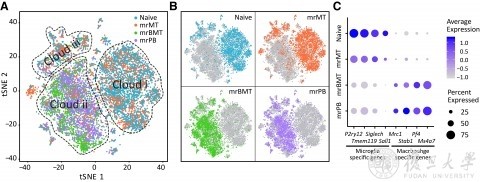
因此,彭勃课题组开发了三种全新的小胶质细胞替换方案,首次在全CNS范围或特定脑区实现高效替换小胶质细胞。该方案为神经退行性病变提供了全新的治疗思路和实现方案。三种方案各自的优势和适用场景将给未来的临床治疗提供多种选择,同时,该方案也是首次在中枢神经系统内实现大规模的细胞移植。


