台大国际团队合作解开DNA复制压力下的保护机制
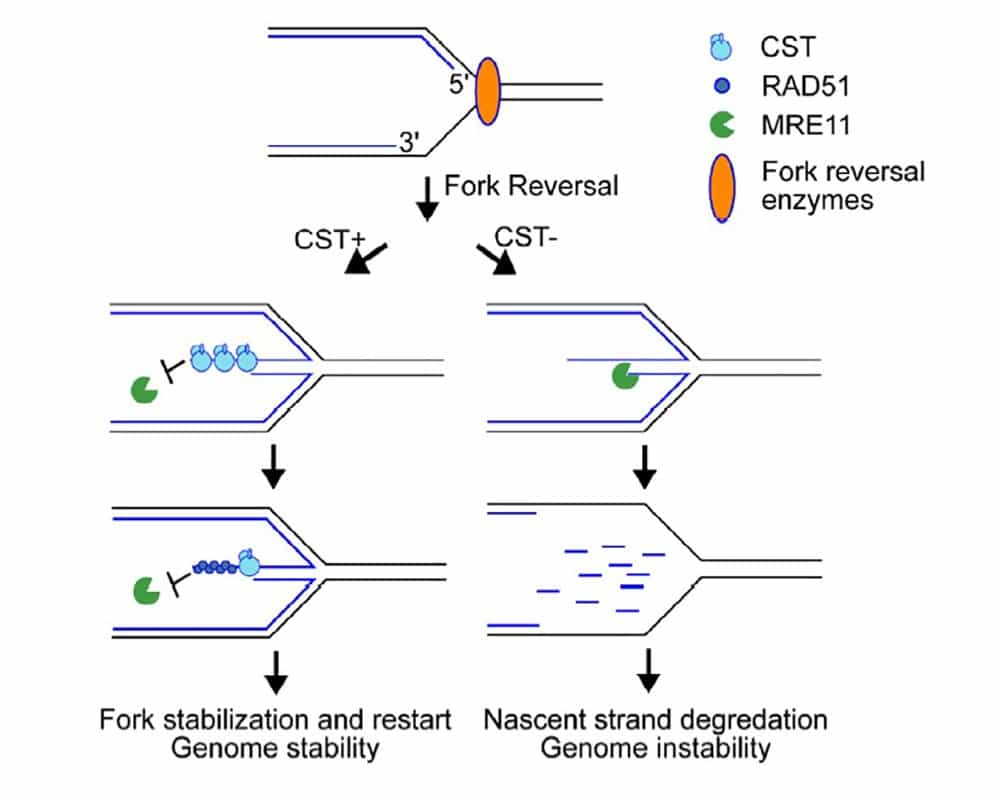
本研究成果于今年(2020)11月19日刊登于The EMBO Journal期刊。有鉴于个体的生长及器官组织的维持和修复,都需由细胞分裂来完成,而细胞分裂的过程,DNA必须复制才能把遗传信息留给下一代。如果DNA复制的过程出现错误,则会发生基因突变进而导致细胞变异、凋亡,甚至演变成癌症。因此,细胞发展出一套精密的保护机制去应对DNA复制压力,来维持基因体的完整性。当DNA遇到复制压力时,复制叉(Replication Fork)会进入停滞状态,并转变成反转复制叉(Reversed Fork)的特殊结构来避免内切核酸酶攻击而断裂,以助于后续的DNA修复与复制的重启。然而反转复制叉的新合成DNA也会因为外切核酸酶MRE11而降解,所以需要可以保护反转复制叉的蛋白来稳定反转复制叉的结构。
本篇研究主要发现一个新参与在复制压力机制的CST蛋白复合体(CTC1-STN1-TEN1),在反转复制叉的保护上扮演了一个重要的角色。本篇第二作者台大生化所博士生李启恒,以人类细胞的蛋白表达系统,成功建立了CST和MRE11的蛋白表现及纯化的方法,并分析其生化功能发现CST可以直接阻挡MRE11外切核酸酶的降解,从而保护反转复制叉的稳定,这也是首次阐明CST具有直接阻挡MRE11降解的生化活性。而通过与美国Weihang Chai教授团队的合作,细胞实验也证明了细胞内的CST也的确具有保护反转复制叉的能力,互相佐证双方的结果。通过细胞和生化的实验,研究团队得以解开了DNA复制压力下的复制叉保护及修复的机制。
本次研究成果突显了团队合作的重要性,即由双方研究专长的互补性,除了能用不同角度的思考来解决问题,更能加速研究的进行,提升研究团队在国际的学术能量。获取更多前沿科技信息访问:https://byteclicks.com
论文全文可见EMBOJ网站:“Human CST complex protects stalled replication forks by directly blocking MRE11 degradation of nascent-strand DNA”


